新規添付文書案の作成

こんにちは。DI営業のKです。
新年あけましておめでとうございます。
昨年は多大なるご厚情を賜り、誠にありがとうございました。
今年の干支である「へび」は、「新しい自分に生まれ変わる」「良い未来、将来」という意味を持っているそうです。
へびが脱皮するように、私も新しいステージへ進めるように精進してまいります!
本年も何卒よろしくお願いいたします。
さて、弊社DI営業では添付文書をはじめとした、様々な資材の作成を行っておりますが、近年では新医薬品の「承認申請用 添付文書案」の作成といった川上業務にも力を入れております。
作成の流れ、作業日数の目安につきましては下記をご参考お願いいたします。
※作業量によって、作業期間は変動いたします。
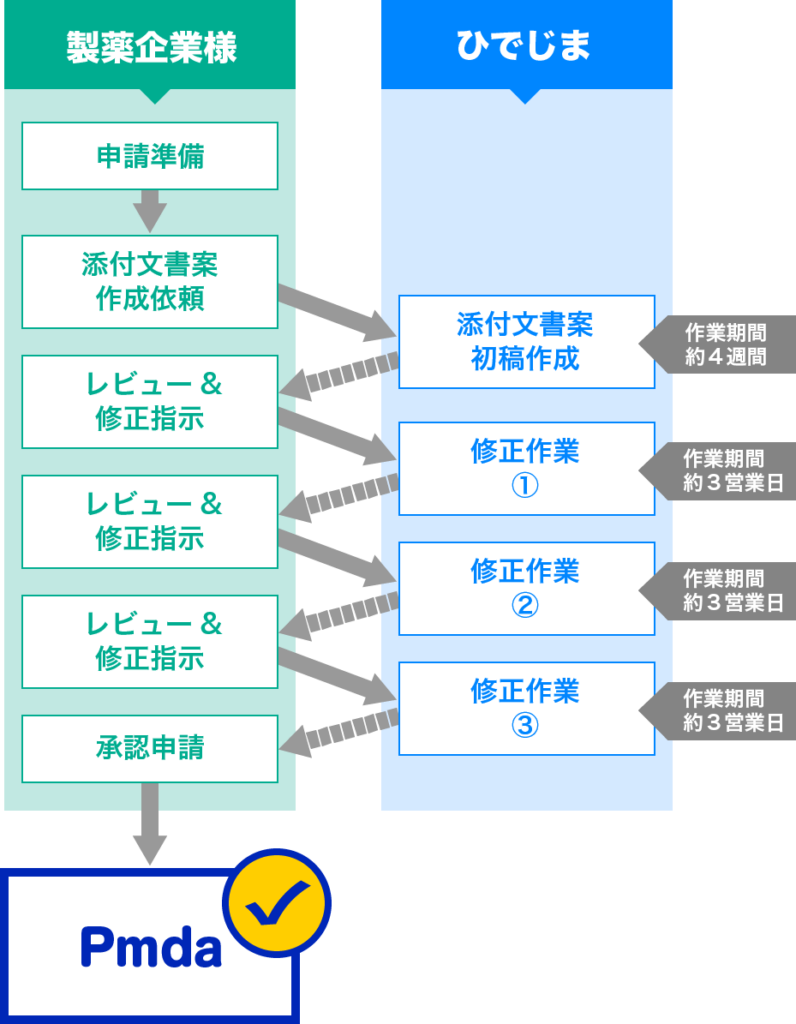
根拠として、下記の資料をご提供いただき作成をいたします。
・CCDS/USPI, EU SPC など/RMP/CTD 2.4, 2.5, 2.6, 2.7/国内類薬の情報としてCTD1.7に記載する製品名など
作成を担当するのは、製薬企業での在籍経験があり、添付文書業務に長く携わった経験豊富な作業者が作成及び、QCを行いますため高品質な添付文書案の作成が可能です。
承認申請後のPMDAとの照会対応も行っておりますため、一度ご相談だけでもいただけますと幸いです。
今後ともよろしくお願いいたします。






