ジェネリックメーカー様向け承認申請資材パック


法改正による作業量の増化
安全対策強化などを目的とした医薬品医療機器等法が2014年より施行され、添付文書の位置付けが見直されました。
さらに承認までの期間では「添付文書案」に加えて「先発品との添付文書対照表」「赤枠付き添付文書案」の提出も求められるようになりました。通常業務を行いながらの承認申請資材作成は、添付文書ご担当者様のご負担の増大となり、多くのジェネリックメーカー様から、作成に苦慮しているとのお声を聞いております。
 承認申請時期の業務の重なり
承認申請時期の業務の重なり
ジェネリック医薬品の承認は2月・8月、申請も2月・8月と、月が決められております。この時期には、承認業務、申請業務、双方の業務を同時に進める必要があります。さらに複数品目を申請する際には、一度に多数の品目を作成しなければなりません。これらの承認申請資材作成は、ご担当者様が通常業務を行いながらの作成となります。お時間がない中で、これらを作成・管理を行うのはご担当者様の大きなご負担ではないでしょうか。



Wordの体裁が整えられない
Wordで添付文書案を作成する際には、段組みの設定・インデントの調整など、細かい箇所にまで気を配らなくてはなりません。さらに表の挿入・文字サイズの統一など、文書全体の複雑なレイアウト調整にお困りではないでしょうか。
 どのような仕様で作成すれば良いかわからない
どのような仕様で作成すれば良いかわからない
対照表は仕様が明確となっていなかったため、ファイル形式・フォーマット・必要項目・記載内容など、どのように作成をするべきか判断に迷われていないでしょうか。






弊社は四半世紀以上にわたり添付文書制作に携わり、メーカー様のお声や市場のニーズを掴みながらサービスの拡充を図って参りました。
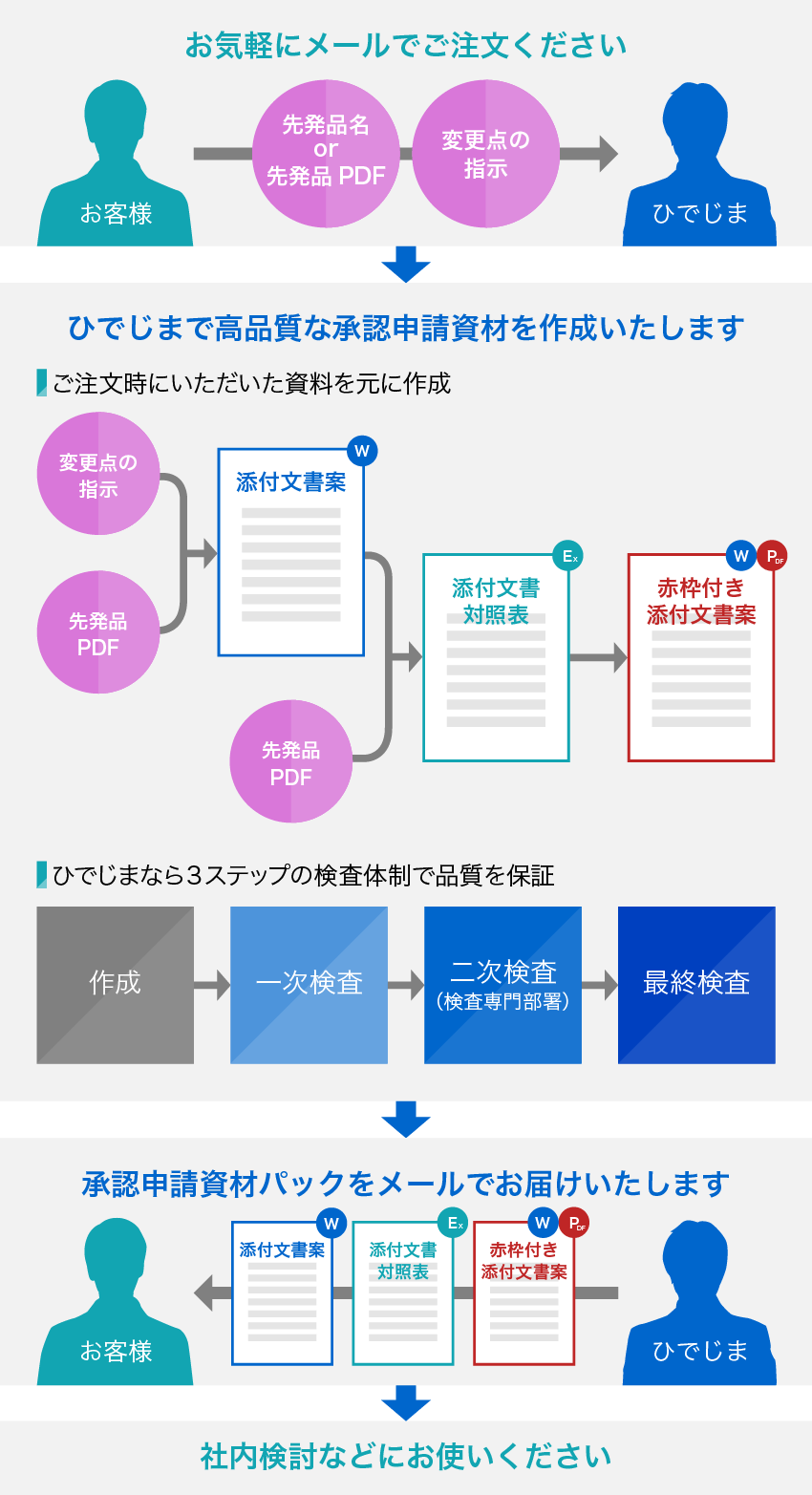
添付文書制作のプロがメーカーご担当者様に代わり、申請時から承認までの期間で必要となる承認申請資材をメーカー様内部で編集可能なファイルにて作成・納品いたします。

添付文書案
(Word)
先発品からの変更点のご指示をいただき、申請時に必要となる添付文書案を完成品と同様のレイアウトで作成いたします。
また短時間での対応が求められる一変承認に備えての既存添付文書のWordも作成いたします。

先発品との添付文書対照表
(Excel)
厚生労働省医薬食品局審査管理課より発出された事務連絡にて推奨されている作成要領(日本ジェネリック製薬協会公表 2015年9月7日付)に基づいて、作成に手間取ることの多い対照表を作成いたします。

赤枠付き添付文書案
(WordまたはPDF)
対照表をもとに先発医薬品と申請品目の相違点を検出し、相違箇所は赤枠で囲いWordまたはPDFにて納品をいたします。相違点として見なさない箇所(句読点や括弧)についてもご報告いたします。
価格
先発医薬品添付文書のページ数により価格が異なる資材がございます。詳細はお問い合わせください。












